PHYSIK → Klasse 9 & 10 → Atomaufbau
Einstieg
- Atomdurchmesser abschätzen Teil 1
Material: 1x Becken mit rechteckiger Grundfläche, 1x Messzylinder, 250g Kichererbsen (getr.)
Vorbereitung: -
 Durchführung: Fülle das Becken mit den Kichererbsen so aus, dass der Boden von genau einer Schicht bedeckt ist. Bestimme anschließend das Volumen der Kichererbsen in dem Becken mithilfe des Messzylinders.
Durchführung: Fülle das Becken mit den Kichererbsen so aus, dass der Boden von genau einer Schicht bedeckt ist. Bestimme anschließend das Volumen der Kichererbsen in dem Becken mithilfe des Messzylinders.
Auswertung:
- Bestimme den Durchmesser einer Kichererbse.
- Überlege dir wie ein analoges Experiment zur Abschätzung des Atomdurchmessers aufgebaut sein muss.
- Atomdurchmesser abschätzen Teil 2
Material: 1x Becherglas, 1x Bärlappsporen, 1x Tropfbürette, 5ml Ölsäure mit Leichtbenzin verdünnt (Verhältnis 1:2000), 1x Maßband
Vorbereitung: Bestimme zunächst das Volumen eines Tropfens der Ölsäure in dem du 0.25cm³ aus der Bürette tropfst und dies durch die Anzahl der Tropfen teilst. Befülle anschließend das Becherglas mit Wasser und bestäube die Oberfläche mit den Bärlappsporen.
 Durchführung:Tropfe genau einen Tropfen der Ölsäure auf die Wasseroberfläche und warte bis das Benzin aus dem Tropfen verdunstet ist. Miss anschließend den Durchmesser des auf der Wasseroberfläche entstandenen Kreises.
Durchführung:Tropfe genau einen Tropfen der Ölsäure auf die Wasseroberfläche und warte bis das Benzin aus dem Tropfen verdunstet ist. Miss anschließend den Durchmesser des auf der Wasseroberfläche entstandenen Kreises.
Messergebnisse: 14 Tropfen für 0.25cm³, Fleckdurchmesser \(d=16.2cm\)
Auswertung:
- Bestimme die Höhe \(h\) des Flecks mithilfe des Zylindervolumens
\[V_{Zyl.}=\pi \cdot r^2\cdot h\]
- Der Ölfleck auf der Wasseroberfläche besteht ebenfalls aus einer Molekülschicht \(C_{17}H_{33}COOH\). Das Molekül kann als annähernd würfelförmig betrachtet werden, bestimme das Volumen eines Moleküls \(V_{Molekül}\).
- Aus wie vielen Atomen \(n\) besteht ein Molekül?
- Auch die Atome im Molkeül sollen als annähernd würfelförmig und gleich groß betrachtet werden. Bestimme das Volumen pro Atom \(V_{Atom}\) und daraus den Durchmesser eines Atoms \(d_{Atom}\).
-
Auch wenn es schön ist den Durchmesser eines Atoms zu kennen, steckt die Physik und ihre Anwendung in nahe zu allen technischen Geräten (Leiter, Halbleiter, etc.) im Aufbau der Atome.
- Arbeite die Geschichte des Atommodells bis 1924 durch. (wenn du magst kannst du dir auch die weiteren Entdeckungen anschauen)
- Fertige eine Skizze zum Rutherfordschen Streuversuch (Video) an und formuliere die zentrale Entdeckung in einem Merksatz. Du kannst die Simulation verwenden um die Vorgänge nochmal zu veranschaulichen.
- Fertige eine Skizze des Atommodells nach 1924 an und beschrifte die zentralen Elemente.
- Atomdurchmesser abschätzen Teil 1Material: 1x Becken mit rechteckiger Grundfläche, 1x Messzylinder, 250g Kichererbsen (getr.)
Vorbereitung: -
Durchführung: Fülle das Becken mit den Kichererbsen so aus, dass der Boden von genau einer Schicht bedeckt ist. Bestimme anschließend das Volumen der Kichererbsen in dem Becken mithilfe des Messzylinders.
Auswertung:- Bestimme den Durchmesser einer Kichererbse.
- Überlege dir wie ein analoges Experiment zur Abschätzung des Atomdurchmessers aufgebaut sein muss.
- Atomdurchmesser abschätzen Teil 2Material: 1x Becherglas, 1x Bärlappsporen, 1x Tropfbürette, 5ml Ölsäure mit Leichtbenzin verdünnt (Verhältnis 1:2000), 1x Maßband
Vorbereitung: Bestimme zunächst das Volumen eines Tropfens der Ölsäure in dem du 0.25cm³ aus der Bürette tropfst und dies durch die Anzahl der Tropfen teilst. Befülle anschließend das Becherglas mit Wasser und bestäube die Oberfläche mit den Bärlappsporen.
Durchführung:Tropfe genau einen Tropfen der Ölsäure auf die Wasseroberfläche und warte bis das Benzin aus dem Tropfen verdunstet ist. Miss anschließend den Durchmesser des auf der Wasseroberfläche entstandenen Kreises.
Messergebnisse: 14 Tropfen für 0.25cm³, Fleckdurchmesser \(d=16.2cm\)
Auswertung:- Bestimme die Höhe \(h\) des Flecks mithilfe des Zylindervolumens \[V_{Zyl.}=\pi \cdot r^2\cdot h\]
- Der Ölfleck auf der Wasseroberfläche besteht ebenfalls aus einer Molekülschicht \(C_{17}H_{33}COOH\). Das Molekül kann als annähernd würfelförmig betrachtet werden, bestimme das Volumen eines Moleküls \(V_{Molekül}\).
- Aus wie vielen Atomen \(n\) besteht ein Molekül?
- Auch die Atome im Molkeül sollen als annähernd würfelförmig und gleich groß betrachtet werden. Bestimme das Volumen pro Atom \(V_{Atom}\) und daraus den Durchmesser eines Atoms \(d_{Atom}\).
-
Auch wenn es schön ist den Durchmesser eines Atoms zu kennen, steckt die Physik und ihre Anwendung in nahe zu allen technischen Geräten (Leiter, Halbleiter, etc.) im Aufbau der Atome.
- Arbeite die Geschichte des Atommodells bis 1924 durch. (wenn du magst kannst du dir auch die weiteren Entdeckungen anschauen)
- Fertige eine Skizze zum Rutherfordschen Streuversuch (Video) an und formuliere die zentrale Entdeckung in einem Merksatz. Du kannst die Simulation verwenden um die Vorgänge nochmal zu veranschaulichen.
- Fertige eine Skizze des Atommodells nach 1924 an und beschrifte die zentralen Elemente.
Aufgaben
- Fertige eine Tabelle mit den dick gedruckten Begriffen aus dem Wissensteil an und ordne ihnen ggf. ihr Formelzeichen zu und ihre Bedeutung.
- Erstelle folgende Atome in der Simulation:
- Neutral: \({}^2_1H\) (Deuterium), \({}^3_1H\) (Tritium), \({}^{17}_9F\)
- 1-fach positiv: \({}^7_3Li\)
- 2-fach negativ: \({}^7_3Li\)
- Beschrifte die dargestellten Atome. Gib außerdem an ob es sich um ein Ion handelt.
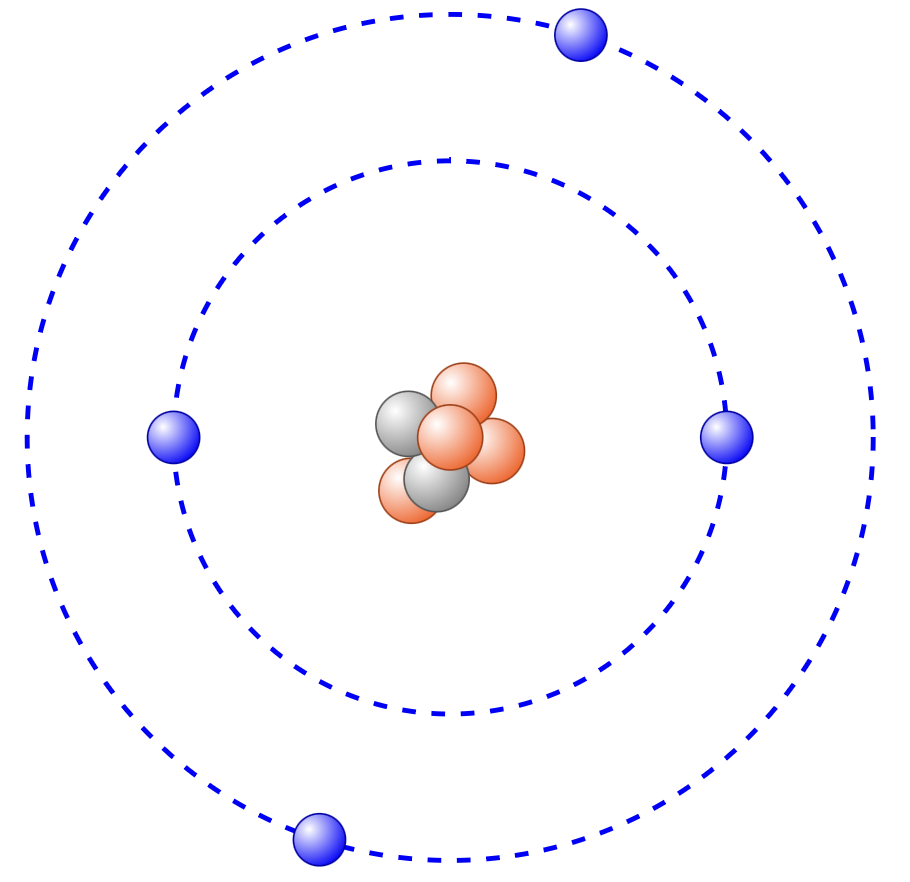
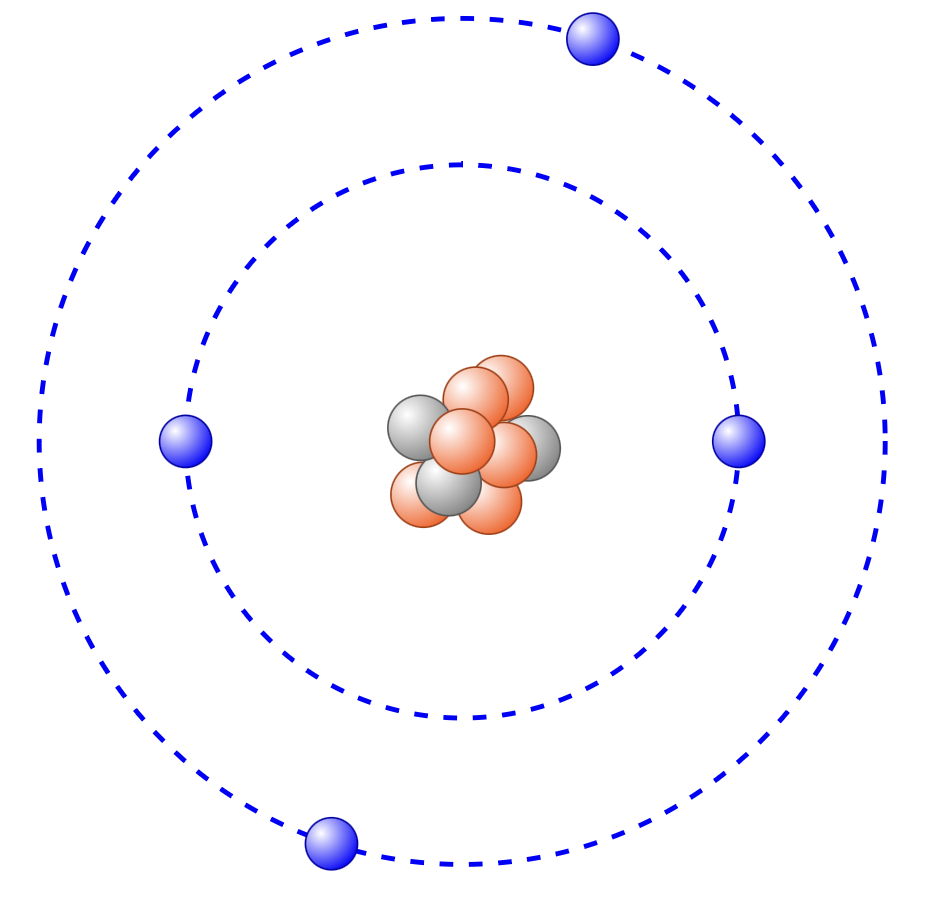
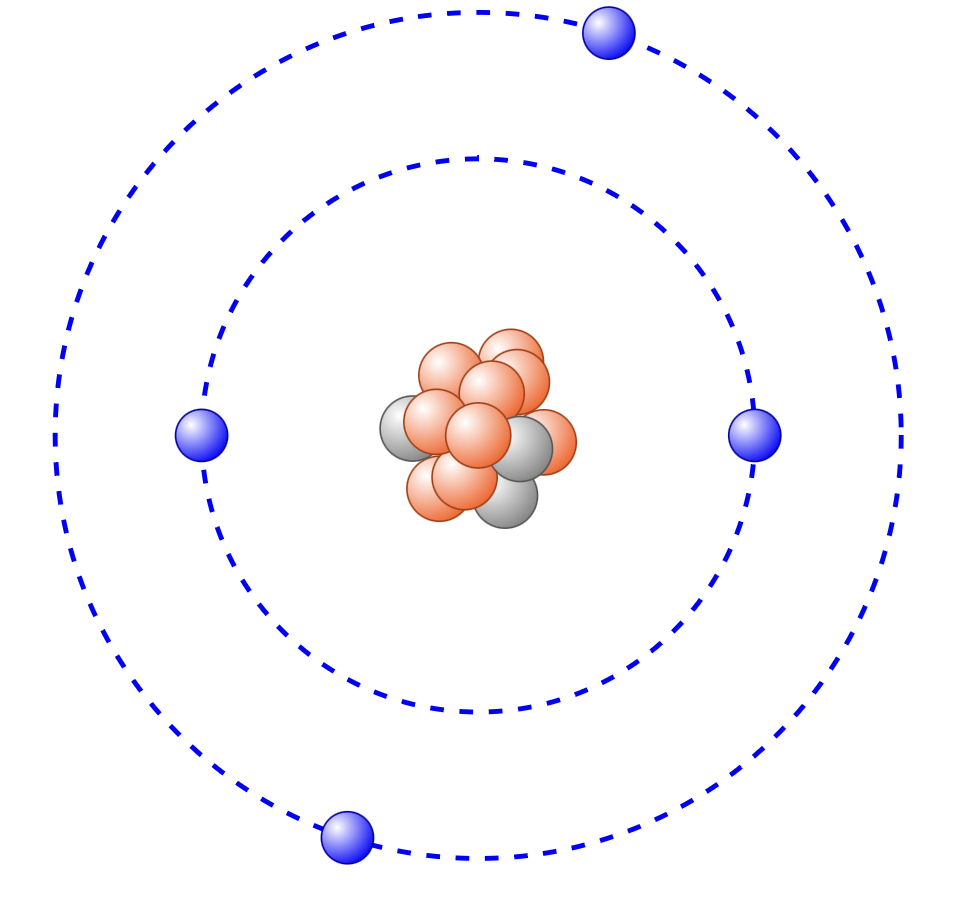
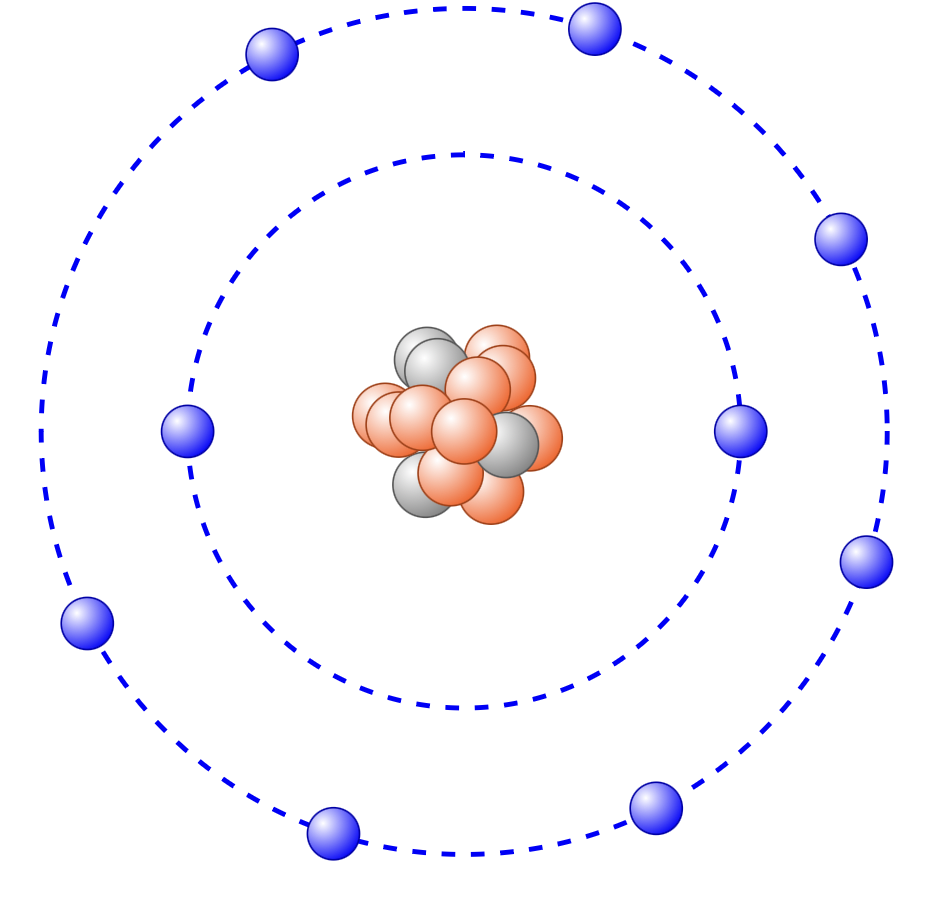
- Fertige eine Tabelle mit den dick gedruckten Begriffen aus dem Wissensteil an und ordne ihnen ggf. ihr Formelzeichen zu und ihre Bedeutung.
- Erstelle folgende Atome in der Simulation:
- Neutral: \({}^2_1H\) (Deuterium), \({}^3_1H\) (Tritium), \({}^{17}_9F\)
- 1-fach positiv: \({}^7_3Li\)
- 2-fach negativ: \({}^7_3Li\)
- Beschrifte die dargestellten Atome. Gib außerdem an ob es sich um ein Ion handelt.



